
Chères consœurs, chers confrères,
L’Assistance Médicale à la Procréation connaît depuis plusieurs années une évolution rapide, portée par des avancées technologiques majeures qui transforment en profondeur nos pratiques. Malgré ces progrès, de nombreuses questions persistent quant à l’optimisation des résultats, à la sélection des gamètes et des embryons, et à la compréhension fine des mécanismes d’implantation.
Dans ce contexte, la journée scientifique des BLEFCO consacrée aux « Approches innovantes en AMP – Cryobiologie et biomarqueurs émergents, des gamètes à l’implantation » a permis de faire le point sur des thématiques au cœur de nos pratiques actuelles et futures. De la vitrification aux nouveaux outils d’évaluation des gamètes et de l’embryon, jusqu’aux biomarqueurs impliqués dans le dialogue embryon-endomètre, ces innovations ouvrent des perspectives prometteuses, tout en soulevant des enjeux d’évaluation, d’appropriation et de pertinence clinique.
À travers cette newsletter, nous avons souhaité partager avec vous les principaux enseignements de cette journée, en mettant en lumière les avancées présentées, mais aussi leurs limites, leurs conditions d’utilisation et leur place dans une pratique fondée sur les données de la science.
Le bureau des BLEFCO vous souhaite une excellente lecture.
Dévitrification et vitrification ultra rapide embryonnaire – Muriel Lopes
La technique de vitrification a révolutionné la cryoconservation non seulement ovocytaire mais aussi embryonnaire dans les laboratoires de fécondation in vitro (FIV). Le réchauffement des blastocystes requiert un temps technique significatif. Cependant plusieurs publications récentes ont démontré l’efficience d’un réchauffement ultra-rapide des blastocystes en une seule étape permettant de réduire le temps technique et d’améliorer la gestion des flux de travail au sein des laboratoires. Cette évolution technique a été mise en place au laboratoire de FIV des Hospices Civils de Lyon. Nous avons évalué la non-infériorité du protocole de réchauffement ultra-rapide des blastocystes versus la méthode de réchauffement standard utilisée en routine, en 3 étapes, en vigueur auparavant. Sur plus de 2000 réchauffements d’embryons vitrifiés réalisés entre 2024 et 2025, les taux de survie, taux de FCS, taux de grossesses biochimiques et évolutives étaient similaires entre le protocole ultra rapide et le protocole standard de réchauffement des blastocystes. Dans notre pratique, le protocole de réchauffement ultra-rapide testé a permis d’optimiser les flux de travail au laboratoire et les différents paramètres étudiés sont équivalents entre les deux protocoles.

Dévitrification et vitrification ultra rapide des ovocytes – Cendrine Siraudin
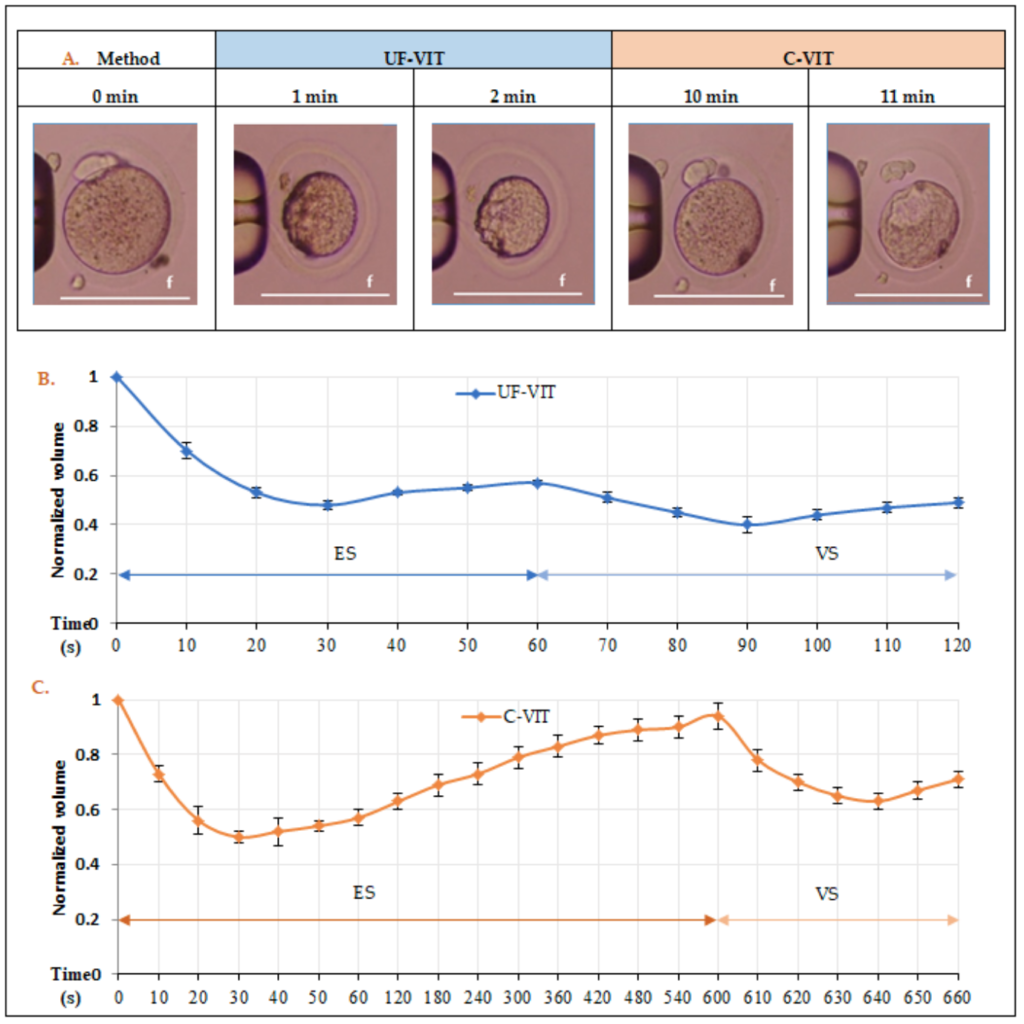
La vitrification ultra-rapide (UFV) associée au réchauffement ultra-rapide (UFW) semble représenter une avancée majeure en cryobiologie ovocytaire. En réduisant fortement les temps d’exposition aux solutions cryoprotectrices (1 minute pour chaque étape), cette méthode limiterait leur toxicité tout en maitrisant le temps passé par les gamètes à température ambiante. La vitrification ultra rapide réduit les variations de volume cellulaire et le stress osmotique, ce qui protègerait mieux les structures internes des ovocytes, comme les mitochondries et le réticulum endoplasmique. Les données récentes publiées par plusieurs équipes étrangères montrent des taux de survie ovocytaire ≥ 95 %, une meilleure progression du développement embryonnaire et des taux de blastulation plus élevés. Cette technique permettrait d’optimiser les performances des laboratoires d’AMP et offrirait des perspectives prometteuses pour la préservation de la fertilité qui révolutionne le flux d’activité de nos centres et nous pousse à revoir nos organisations. Une précaution particulière doit cependant être prise pour les situations hybrides : réchauffer des ovocytes de manière ultra-rapide lorsqu’ils ont été vitrifiés de manière standard ne semble pas favorable. Enfin, il est important pour chaque laboratoire d’évaluer ses propres résultats et indicateurs techniques car le taux de survie seul semble insuffisant pour évaluer l’inocuité de la technique. Une surveillance des indicateurs d’évolutivité embryonnaire et des issues de grossesses est encore nécessaire.
Nouveaux marqueurs de la qualité ovocytaire – Marie Hélène Verlhac
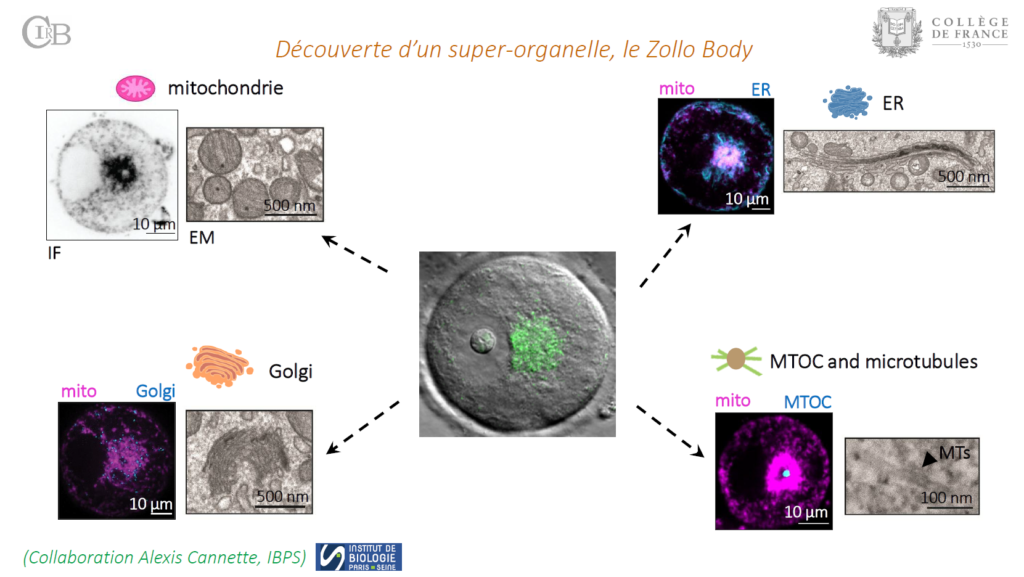
Les ovocytes mammifères présentent une phase de croissance prolongée, au cours de laquelle la transcription diminue progressivement. Pour soutenir les divisions méiotiques et le développement embryonnaire précoce, les ovocytes en croissance doivent accumuler des réserves maternelles et réguler étroitement la traduction. À l’aide de l’immunofluorescence, de la spectrométrie de masse, de la microscopie électronique, du séquençage d’ARN et de l’imagerie ex vivo de coupes de tissu ovarien vivant, nous avons identifié un nouveau compartiment cellulaire transitoire dans les ovocytes de souris en fin de croissance, que nous avons nommé « corps de Zollo ». Bien qu’il ressemble au corps de Balbiani observé dans les ovocytes primordiaux de nombreuses espèces de vertébrés, le corps de Zollo apparaît à un stade plus tardif et présente une traduction naissante et un enrichissement en phospho-mTOR. La supinoxine (inhibiteur de Ddx5) dissout rapidement le corps de Zollo et arrête la croissance des follicules et des ovocytes dans les coupes de tissu ovarien en culture. Ainsi, le corps de Zollo est un compartiment transitoire associé à la traduction, nécessaire à la croissance normale des follicules et des ovocytes.
Nouveaux marqueurs de la qualité des spermatozoïdes – Nicolas Gatimel
Le spermogramme ne permet pas à lui seul d’explorer certaines anomalies structurales et fonctionnelles du spermatozoïde, susceptibles d’expliquer des infertilités dites « inexpliquées » ou certains échecs en AMP d’origine masculine. Dans ce contexte, les biomarqueurs spermatiques émergents permettent aujourd’hui d’aller au-delà des paramètres classiques en explorant des dimensions fonctionnelles essentielles. Les marqueurs de qualité nucléaire et épigénétique, tels que la méthylation de l’ADN ou la longueur des télomères, apportent des informations sur l’intégrité du génome et ses implications pour le développement embryonnaire. Les micro-ARN spermatiques et certains marqueurs enzymatiques, comme la phospholipase C zêta impliquée dans l’activation ovocytaire, constituent également des pistes prometteuses. Toutefois, leur utilisation en pratique clinique reste limitée par un niveau de validation encore insuffisant et hétérogène. D’autres biomarqueurs de la qualité spermatique sont actuellement proposés avec un intérêt clinique plus avancé, tels que les tests de fragmentation de l’ADN spermatique ou l’analyse des déficités des canaux calciques. Bien que prometteurs, ces derniers reposent encore sur un niveau de preuve limité et leur place dans la stratégie diagnostique et thérapeutique reste à préciser.

Quoi de neuf en génétique de l’infertilité – Xavier Pollet Villard
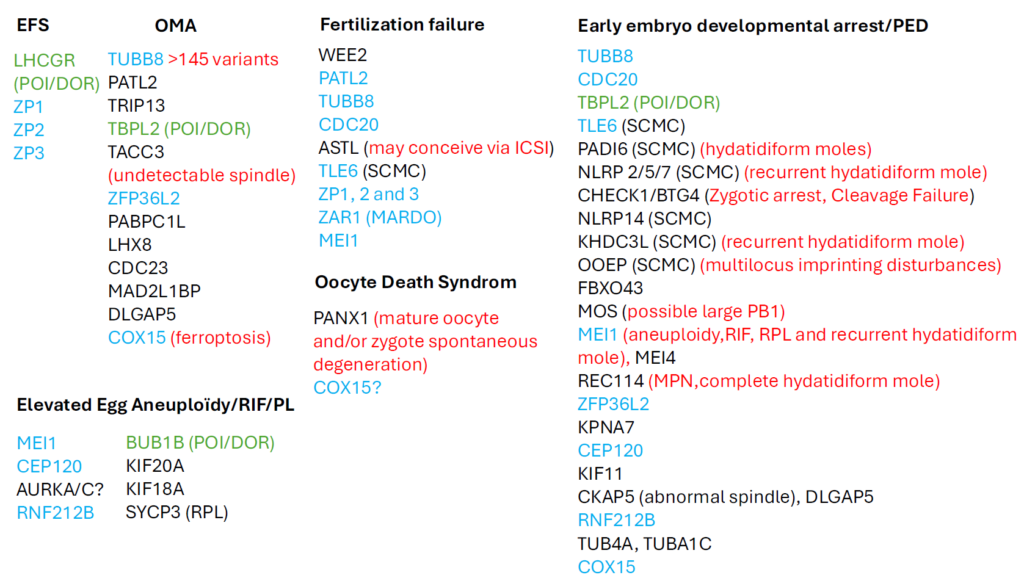
Le bilan étiologique des infertilités féminines et masculines n’aboutit pas toujours à une cause clairement identifiée ; chez l’homme, une part importante des anomalies du spermogramme reste inexpliquée en pratique. Dans les formes sévères, notamment en contexte de consanguinité, le séquençage de l’exome et les études familiales ont mis en évidence des causes monogéniques. Chez l’homme, des variants pathogènes sont décrits dans les hypogonadismes hypogonadotropes congénitaux, l’agénésie des canaux déférents, certaines tératozoospermies monomorphes et l’azoospermie non obstructive. Chez la femme, des variants de gènes effecteurs maternels (MEG) sont impliqués dans des phénotypes sévères en FIV, allant de l’échec de maturation ovocytaire à l’échec de fécondation ou à l’arrêt du développement embryonnaire, regroupés dans OMIM sous le phénotype OZEMA. En l’absence de consensus sur les indications du séquençage, la répétition d’échecs inattendus et certains tableaux évocateurs (p. ex. syndrome de mort ovocytaire lié à PANX1) doivent alerter. D’autres variants peuvent se manifester par une augmentation d’aneuploïdies, des échecs d’implantation ou des fausses couches. Par ailleurs, la susceptibilité polygénique est démontrée pour certaines causes, notamment le SOPK, et la pharmacogénomique pourrait guider l’individualisation des stimulations. Enfin, le séquençage à lecture longue ouvre des perspectives (variants structuraux, accès au génome entier, méthylome) tout en posant des défis d’interprétation, d’éthique et de conseil génétique.
Dialogue au coeur de l’implantation – Kamila Kolanska
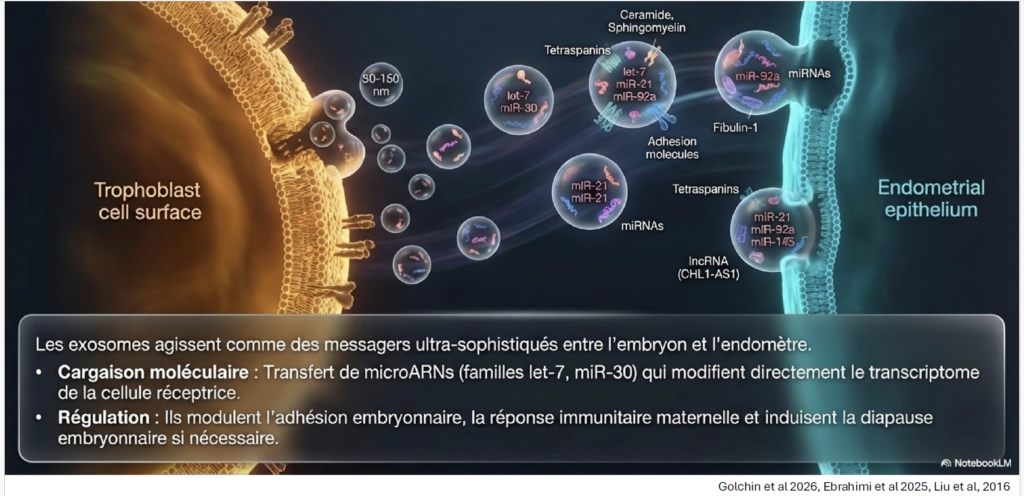
L’implantation embryonnaire repose sur un dialogue fin et dynamique entre l’embryon et l’endomètre. L’embryon, bien que doté de capacités intrinsèques de développement, constitue un élément semi-allogénique qui doit être reconnu et toléré par l’organisme maternel. Cette interaction repose sur une communication complexe impliquant des signaux précoces tels que l’hCG, des vésicules extracellulaires, ainsi que de nombreuses cytokines et chimiokines. L’endomètre, de son côté, doit être dans un état de réceptivité optimal, reposant sur un équilibre immunitaire subtil, notamment impliquant les cellules NK, mais aussi sur des facteurs vasculaires et du microbiote.
Des altérations de ce dialogue, comme dans certains profils immunitaires ou en cas d’endométrite chronique, peuvent contribuer aux échecs d’implantation répétés. Parallèlement, de nouveaux modèles expérimentaux innovants (organoïdes endométriaux, dispositifs microfluidiques “implantation-on-a-chip”) permettent aujourd’hui de mieux décrypter ces interactions. L’ensemble de ces avancées contribue à affiner la compréhension des mécanismes de l’implantation et ouvre des perspectives vers des stratégies d’exploration et de prise en charge plus individualisées en AMP.
CONCLUSION
De la cryobiologie aux biomarqueurs émergents, de l’évaluation des gamètes à la compréhension du dialogue embryon-endomètre, les innovations en AMP redessinent progressivement nos pratiques et ouvrent de nouvelles perspectives pour améliorer les chances de succès.
Ces avancées, prometteuses, nécessitent toutefois une appropriation raisonnée, fondée sur une analyse rigoureuse de leurs bénéfices, de leurs limites et de leur place réelle dans les parcours de soins.
Les BLEFCO, au sein de la FFER, s’engagent à accompagner ces évolutions en promouvant une AMP innovante, critique et fondée sur les preuves, au service des patients et de leurs projets parentaux.



